Глицерин — Википедия
Глицери́н (от греч. γλυκερός — сладкий) — органическое соединение, простейший представитель трёхатомных спиртов с формулой C3H5(OH)3{\displaystyle {\ce {C3H5(OH)3}}}. Представляет собой вязкую прозрачную жидкость со сладким вкусом.
Синонимы: глицерóл, пропантриол-1,2,3.
Бесцветная вязкая жидкость без запаха. Сладкий на вкус, отчего и получил своё название (греч. γλυκερός — сладкий). Имеет молярную массу 92,09 г/моль, относительную плотность d420{\displaystyle d_{4}^{20}} = 1,260, коэффициент преломления nD20{\displaystyle n_{D}^{20}} = 1,4740. Температура плавления составляет 17,9 °C, кипит при 290 °C, частично при этом разлагаясь. Гигроскопичен, поглощает воду из атмосферы в количестве до 40 % от собственной массы. С водой, метанолом, этанолом, ацетоном смешивается в любых пропорциях, но не растворим в эфире и хлороформе, хотя и способен растворяться в их смесях с этанолом[2].
При растворении глицерина в воде выделяется теплота и происходит контракция — уменьшение объёма раствора. Смеси глицерина с водой обладают температурой плавления значительно более низкой, чем каждое из веществ по отдельности, например, при массовом содержании глицерина в 66,7 % его смесь с водой будет замерзать при −46,5 °C[2].
Образует азеотропы с нафталином, его производными и рядом других веществ[2].
Химические свойства глицерина типичны для многоатомных спиртов.
Взаимодействие глицерина с галогеноводородами или галогенидами фосфора ведёт к образованию моно- и дигалогенгидринов.
Глицерин этерифицируется карбоновыми и минеральными кислородосодержащими кислотами с образованием соответствующих сложных эфиров. Так, с азотной кислотой глицерин образует тринитрат — нитроглицерин (получен в 1847 г. Асканио Собреро), использующийся в настоящее время в производстве бездымных порохов.
При дегидратации он образует токсичный акролеин:
- HOCh3CH(OH)−Ch3OH⟶h3C=CH−CHO+2h3O{\displaystyle {\ce {HOCh3CH(OH)-Ch3OH -> h3C=CH-CHO + 2h3O}}},
и окисляется до глицеринового альдегида Ch3OHCHOHCHO{\displaystyle {\ce {Ch3OHCHOHCHO}}}, дигидроксиацетона Ch3OHCOCh3OH{\displaystyle {\ce {Ch3OHCOCh3OH}}} или глицериновой кислоты Ch3OHCHOHCOOH{\displaystyle {\ce {Ch3OHCHOHCOOH}}}.
Сложные эфиры глицерина и высших карбоновых кислот — жиры являются важными метаболитами, существенное биологическое значение также имеют фосфолипиды — смешанные глицериды фосфорной и карбоновых кислот.
Глицерин впервые был получен в 1779 году Карлом Вильгельмом Шееле при омылении жиров в присутствии оксидов свинца [3]. Основную массу глицерина получают как побочный продукт при омылении жиров[4].
Большинство синтетических методов получения глицерина основано на использовании пропилена в качестве исходного продукта. Хлорированием пропилена при 450—500 °С получают аллилхлорид, при присоединении к последнему хлорноватистой кислоты образуются хлоргидрины, например, Ch3ClCHOHCh3Cl{\displaystyle {\ce {Ch3ClCHOHCh3Cl}}}, которые при омылении щёлочью превращаются в глицерин.
На превращениях аллилхлорида в глицерин через дихлоргидрин или аллиловый спирт основаны другие методы. Известен также метод получения глицерина окислением пропилена в акролеин; при пропускании смеси паров акролеина и изопропилового спирта через смешанный ZnO{\displaystyle {\ce {ZnO}}} — MgO{\displaystyle {{\ce {MgO}}}} катализатор образуется аллиловый спирт. Он при 190—270 °C в водном растворе перекиси водорода превращается в глицерин.
Глицерин можно получить также из продуктов гидролиза крахмала, древесной муки, гидрированием образовавшихся моносахаридов или гликолевым брожением сахаров. Также глицерин получается в качестве побочного продукта при производстве биотоплива.
Производные глицерина и их место в обмене веществ живых организмов[править | править код]
Глицериды[править | править код]
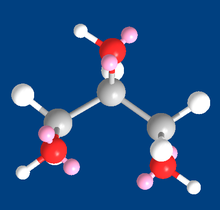 Глицерин (3D модель), показаны атомы и электронные пары при атомах кислорода (розовый цвет)
Глицерин (3D модель), показаны атомы и электронные пары при атомах кислорода (розовый цвет)Триглицериды являются производными глицерина и образуются при присоединении к нему высших жирных кислот. Триглицериды являются важными компонентами в процессе обмена веществ в живых организмах.
Жиры и масла гидрофобны и нерастворимы в воде, так как гидроксильные группы глицерина заменены малополярными остатками жирных кислот.
Область применения глицерина разнообразна: пищевая промышленность, табачное производство, электронные сигареты, медицинская промышленность, производство моющих и косметических средств, сельское хозяйство, текстильная, бумажная и кожевенная отрасли промышленности, производство пластмасс, лакокрасочная промышленность, электротехника и радиотехника (в качестве флюса при пайке).
Глицерин относится к группе стабилизаторов, обладающих свойствами сохранять и увеличивать степень вязкости и консистенции пищевых продуктов. Зарегистрирован как пищевая добавка Е422, и используется в качестве эмульгатора, при помощи которого смешиваются различные несмешиваемые смеси.
Поскольку глицерин хорошо поддается желированию и горит без запаха и чада, его используют для изготовления высококачественных прозрачных свечей и основы для жидкости, используемой в дым-машинах.
Также глицерин используется при изготовлении динамита[5].
В последние годы глицерин используется, наряду с пропиленгликолем, в качестве основного компонента для приготовления жидкости и картриджей для электронных сигарет.
Используется в криобиологии и крионике как основной компонент популярных проникающих криопротекторов для криоконсервирования анатомических препаратов, биологических тканей и организмов.

Глицерин — Циклопедия
Удивительные свойства глицеринаГлицерин — трёхатомный спирт.
Химическая формула 2C3H5(OH)3.
Глицерин был открыт в 1783 году шведским химиком К.Шееле, который показал, что фрагменты этого соединения составляют основу всех природных жиров и назвал его «сладкое начало масел», поскольку продукт обладал сладким вкусом.
В 1813 году французским химиком М.Шеврелем было установлено, что под действием воды (катализаторы: кислота или щелочь) происходит расщепление жиров с образованием глицерина и высших карбоновых кислот. Им впервые было дано название «глицерин» одному из продуктов, который образуется в данном процессе («глицерос» — сладкий).
Синтез глицерина впервые был проведен в 1873 году французским химиком и минералогом Ш. Фриделем.
[править] Физические свойства
Чистый глицерин представляет собой прозрачную, бесцветную, очень густую, вязкую, сиропообразную, без запаха, тяжелее воды и неядовитую сладковатую на вкус жидкость.
Глицерин обладает способностью поглощать влагу из воздуха и удерживать ее. На воздухе может впитать до 50 % воды.[1] Поэтому глицериновая капля на руке дает впечатление легкого нагрева.
Удельный вес химически чистого глицерина при 15 °С составляет 1,26469.
Молекулярная масса 92,09 г/моль.
При обычном атмосферном давлении глицерин кипит при 290 °C и частично разлагается; под пониженным давлением его можно перегнать, не разложив.[1] Смешивается с водой в любой пропорции. Температура вспышки глицерина составляет 150 °C, температура самовоспламенения — 362 °C. При нагревании глицерин быстро испаряется, а в обычных условиях глицерин не летуч.
Глицерин обладает способностью растворять различные минеральные соли, из-за чего чистый глицерин добывается главным образом путем перегонки.[1]
От сильного и длительного охлаждения глицерин кристаллизуется; температура плавления кристаллов — 20 °C.
Плотность 1,261 г/см3 при 20 °C. Показатель преломления N D = 1,4735 при 20 °C. диэлектрическая проницаемость ε = 42,5 при 25 °C. дипольный момент молекулы в газовом состоянии μ = 2,56 Дб.[2]
[править] Химические свойства
С водой глицерин смешивается во всех пропорциях, причем объем такого раствора будет немного меньше суммы первоначальных объемов воды и глицерина. Во всех пропорциях смешивается с этанолом. Нерастворим в жирах, масле, бензине, хлороформе. [1]
Наличие гидроксильных групп обусловливает сходство глицерина в одноатомных спиртов, он вступает в те же реакции, но с участием трех гидроксильных групп.
Реакции полного окисления (горения) происходит, как и у других органических веществ, с образованием углекислого газа и воды.
Глицерин вступает в реакцию замещения с металлическим натрием, которая сопровождается выделением водорода.
Реакция с гидроксидами металлов. В отличие от одноатомных спиртов, многоатомные взаимодействуют с гидроксидами щелочных и металлических элементов.
[править] Реакции
Горение:
- 2C3H5(OH)3 + 7O2 → 6CO2 + 8H2O
Взаимодействие с металлическим натрием:
- 2C3H5
Взаимодействие с нерастворимыми основаниями:
Глицерин высокой степени чистоты (не менее 98 %) получают путем алкоголиза растительных жиров с применением вакуум-ректификации.
До разработки синтетических методов глицерин получали щелочным омылением жиров. При этом образуется мыло с водным раствором глицерина. Мыло отделяют путем высаливания с помощью хлорида натрия, а глицерин получают путем повторного сгущения и кристаллизации осажденного хлорида натрия. Полученный 80 % глицерин темного цвета очищается перегонкой и обработкой активированным углем.
Существует ферментативный метод получения глицерина.
Другой метод основан на гидролитическом расщеплении углеводов (крахмала, древесной муки и сахара, особенно тростникового), приводит к образованию смеси глицерина с другими гликолями.
Также глицерин образуется при производстве биотоплива.
[править] Применение в промышленности
В промышленности его получают главным образом при гидролитическом расщеплении жиров. Глицерин выпускают трех видов — сырой, дистиллированный и технически чистый. В косметике разрешено применение двух последних. Глицерин гигроскопичен. Благодаря свойству поглощать из воздуха до 40-50 % воды по отношению к его начальной массе, он получил широкое распространение в косметике как вещество, которое быстро отбирает воду из животной и растительной ткани. Он применяется почти во всех косметических препаратах как смягчающее средство и является одним из основных видов сырья для изготовления зубных паст. Он не засыхает, не горчит, замерзает при очень низких температурах и поэтому применяется как вещество, препятствующее высыханию и замерзанию косметических изделий.
Глицерин используется в парфюмерии и фармации как смягчающим средство или основа мазей, добавка к маслу, в пищевой промышленности — в качестве добавки к напиткам. Спиртовой раствор тринитроглицерина оказывает сосудорасширяющее действие и в виде лекарств используется при сердечных заболеваниях. Глицерин, его олигомеры и полимеры предложены в качестве средств, которые сохраняют свежесть пищевых продуктов.
В кожевенном производстве и текстильной промышленности применяется для обработки пряжи и кожи с целью их смягчения и предоставления эластичности. Глицерин применяется в табачной промышленности, при производстве полиуретанов, резины, фанеры, красителей, чернил и паст, зубной пасты, эмульгаторов, фотографических и других материалов.
Применяется как одно из составных веществ в жидкостях для электронных испарителей.
С глицерина добывают взрывчатое вещество тринитроглицерин, который используется для изготовления динамита.
Глицерин в качестве кормовой добавки повышает надои молока.[3]
- ↑ 1,01,11,21,3 В. М. Полищук. Животные и растительные жиры в качестве сырья для производства биодизеля (обобщение опыта). Научный вестник Национального университета биоресурсов и природопользования Украины. Сборник научных трудов — 2010, Вып. 144.
- ↑ Физические константы приведены по изданию: А. Гордон, Р. Форд. Спутник химика. Физико-химические свойства, методики, библиография. Москва: Мир, 1976, с.20-21
- ↑ Печатный М. Ф., Яремчук А. С., Мазур И. Развитие комплекса биотехнологий — главный путь развития аграрного сектора Украины // Научные труды Института биоэнергетических культур и сахарной свеклы. Сборник научных трудов. — 2011, № 12
Глицерин: кто он и откуда
Наряду с водой, глицерин – один из самых часто встречающихся компонентов косметики. Он имеет долгую историю использования и отличный профиль безопасности.
По своей природе это трехатомный спирт (при этом совершенно неважно, из чего этот самый глицерин получен и каким методом, он все равно был и остается трехатомным спиртом!), внешне – бесцветная, прозрачная сиропообразная жидкость.
Иногда в Интернете можно найти утверждения следующего плана: глицерин (или Glycerin) – это полезный растительный глицерин, а глицерол (Glycerol) – жутко опасный синтетический глицерин. В действительности это утверждение порождено незнанием англоязычной терминологии (и, отчасти, возможно, маркетинговыми соображениями, куда же без них). В английском языке слово Glycerol относится к глицерину как химическому веществу, тогда как термин Glycerin – это название для косметического [1] или фармакопейного ингредиента, представляющего собой высокочистый водный раствор глицерина с содержанием основного вещества не менее 95%. В русском же языке подобные терминологические различия отсутствуют, и правильным термином является именно «глицерин», тогда как «глицерол» — просто бессмысленная калька с английского.
Глицерин в природе встречается главным образом в составе сложных эфиров с высшими жирными кислотами, то есть, масел и жиров. Глицерин — естественный компонент многих продуктов ферментации (вино, пиво, хлеб)[2]. Он также является важным интермедиатом метаболизма живых существ.
Существует промышленный способ производства глицерина из пропилена, однако с развитием олеохимии[3] этот способ совершенно утратил значение – во всяком случае, в производстве фармакопейного глицерина, используемого и в косметике: ведь глицерин в больших количествах образуется в результате гидролиза[4] или переэтерификации растительных масел, главным образом кокосового и пальмового. Эти масла недороги, объемы промышленной переработки очень велики, и образующийся в результате глицерин, даже не будучи целевым продуктом, ввиду больших количеств и несложной процедуры очистки приобрел немалое коммерческое значение. Олеохимический глицерин (то есть, тот самый, который принято называть «растительным»), вопреки приведенному выше утверждению, совсем недорог, и ни химически, ни биохимически молекулы глицерина, независимо от способа его получения, не отличимы друг от друга. Так что все попытки построить маркетинговую концепцию на «таком дорогом, но таком благотворном растительном (натуральном) глицерине, используемом только в нашей косметике, в то время как остальные используют дешевый синтетический» — увы, не более чем обман: весь используемый в косметике глицерин дешев и имеет растительное происхождение. Несколько дороже будет глицерин, одобренный стандартами NATRUE, COSMOC и т.п., но не потому, что он какой-то более натуральный, а в силу бОльших затрат на выращивание сырья по определенным агротехникам и на подтверждение соответствия экологическому стандарту.
Точно так же несостоятельны и утверждения наподобие следующего: «Для того, чтобы глицерин оказывал благотворное действие на кожу, он, во-первых, должен быть натуральным, во-вторых, в правильной пропорции сочетаться с другими натуральными компонентами. Если же вы не хотите покупать органическую косметику, лучше пробуйте найти крем без глицерина вообще». Увы, и здесь лукавый маркетинг: глицерин в косметике, позиционируемой как натуральная, с точки зрения что химии, что вашего организма, точно такой же, что и в «обыкновенном» креме, а для достижения положительного эффекта вовсе не обязательно сочетать его исключительно с натуральными ингредиентами.
Впрочем, оставим пустопорожние разговоры о кардинальных отличиях «натурального» глицерина от «его синтетического аналога» на совести их авторов – все это плоды плохого знания химии вообще и биохимии в частности, плюс банальный меркантильный интерес. Важнее другое: ведь откуда-то берутся все эти настойчиво распространяемые истории об «иссушающем» действии глицерина. Вопрос значительно сложнее, чем кажется на первый взгляд.
[1] Узаконенное международной номенклатурой косметических ингредиентов.
[2] Странно, что никому еще не пришло на ум пугать «иссушением организма изнутри» всех тех, кто ест хлеб: ведь глицерин (ужас!) попадает на слизистые, и уж конечно, следуя своей коварной природе, «вытягивает из них воду»! Смысла в этой страшилке, естественно, ничуть не больше, чем в слухах об «иссушающем» действии глицерина в составе косметики, но что с того?
[3] Олеохимия — промышленная химическая переработка растительных масел.
[4] Омыление растительных масел, по сути – частный случай гидролиза.
Глицерин — Википедия
Глицери́н (глицерóл, пропантриол-1,2,3) — простейший представитель трёхатомных спиртов с формулой C3H5(OH)3. Представляет собой вязкую прозрачную жидкость.
Свойства
Глицерин — бесцветная, вязкая, очень гигроскопичная жидкость, смешивается с водой в любых пропорциях. Сладкий на вкус, отчего и получил своё название (др.-греч. γλυκός — сладкий). В соединении с пропиленгликолем становится более текучим.
Химические свойства глицерина типичны для многоатомных спиртов.
Взаимодействие глицерина с галогеноводородами или галогенидами фосфора ведёт к образованию моно- и дигалогенгидринов.
Глицерин этерифицируется карбоновыми и минеральными кислородосодержащими кислотами с образованием соответствующих сложных эфиров. Так, с азотной кислотой глицерин образует тринитрат — нитроглицерин (получен в 1847 г. Асканьо Собреро), использующийся в настоящее время в производстве бездымных порохов.
При дегидратации он образует токсичный акролеин:
- HOCH2CH(OH)-CH2OH →{\displaystyle \to } H2C=CH-CHO + 2 H2O,
и окисляется до глицеринового альдегида CH2OHCHOHCHO, дигидроксиацетона CH2OHCOCH2OH или глицериновой кислоты CH2OHCHOHCOOH.
Сложные эфиры глицерина и высших карбоновых кислот — жиры являются важными метаболитами, важное биологическое значение играют также фосфолипиды — смешанные глицериды фосфорной и карбоновых кислот.
Получение
Глицерин впервые был получен в 1779 году Карлом Вильгельмом Шееле при омылении жиров в присутствии окислов свинца[2]. Основную массу глицерина получают как побочный продукт при омылении жиров[3].
Большинство синтетических методов получения глицерина основано на использовании пропилена в качестве исходного продукта. Хлорированием пропилена при 450—500 °С получают аллилхлорид, при присоединении к последнему хлорноватистой кислоты образуются хлоргидрины, например, CH2ClCHOHCH2Cl, которые при омылении щёлочью превращаются в глицерин.
На превращениях аллилхлорида в глицерин через дихлоргидрин или аллиловый спирт основаны другие методы. Известен также метод получения глицерина окислением пропилена в акролеин; при пропускании смеси паров акролеина и изопропилового спирта через смешанный ZnO — MgO катализатор образуется аллиловый спирт. Он при 190—270 °C в водном растворе перекиси водорода превращается в глицерин.
Глицерин можно получить также из продуктов гидролиза крахмала, древесной муки, гидрированием образовавшихся моносахаридов или гликолевым брожением сахаров. Также глицерин получается в качестве побочного продукта при производстве биотоплива.
Производные глицерина и их место в обмене веществ живых организмов
Глицериды
Глицерин (3D модель), показаны атомы и электронные пары при атомах кислорода (розовый цвет)Триглицериды являются производными глицерина и образуются при присоединении к нему высших жирных кислот. Триглицериды являются важными компонентами в процессе обмена веществ в живых организмах.
Жиры и масла гидрофобны и нерастворимы в воде, так как гидроксильные группы глицерина заменены малополярными остатками жирных кислот.
Применение
Область применения глицерина разнообразна: пищевая промышленность, табачное производство, электронные сигареты, медицинская промышленность, производство моющих и косметических средств, сельское хозяйство, текстильная, бумажная и кожевенная отрасли промышленности, производство пластмасс, лакокрасочная промышленность, электротехника и радиотехника (в качестве флюса при пайке).
Глицерин относится к группе стабилизаторов, обладающих свойствами сохранять и увеличивать степень вязкости и консистенции пищевых продуктов. Зарегистрирован как пищевая добавка Е422, и используется в качестве эмульгатора, при помощи которого смешиваются различные несмешиваемые смеси.
Поскольку глицерин хорошо поддается желированию и горит без запаха и чада, его используют для изготовления высококачественных прозрачных свечей.
Также глицерин используется при изготовлении динамита[4].
В последние годы глицерин используется, наряду с пропиленгликолем, в качестве основного компонента для приготовления жидкости и картриджей для электронных сигарет.
Используется в криобиологии и крионике как основной компонент популярных проникающих криопротекторов для криоконсервирования анатомических препаратов, биологических тканей и организмов.
Примечания
Ссылки
Глицерин — это… Что такое Глицерин?
Глицери́н (1,2,3-тригидроксипропан; 1,2,3-пропантриол) (гликос — сладкий) химическое соединение с формулой HOCH2CH(OH)-CH2OH или C3H5(OH)3. Простейший представитель трёхатомных спиртов. Представляет собой вязкую прозрачную жидкость.
Физические свойства
Глицерин — бесцветная, вязкая, гигроскопичная жидкость, неограниченно растворимая в воде. Сладкий на вкус, отчего и получил своё название (гликос — сладкий). Хорошо растворяет многие вещества.
Химические свойства
Химические свойства глицерина типичны для многоатомных спиртов.
Взаимодействие глицерина с галогеноводородами или галогенидами фосфора ведёт к образованию моно- и дигалогенгидринов.
Глицерин этерифицируется карбоновыми и минеральными кислотами с образованием соответствующих эфиров. Так, с азотной кислотой глицерин образует тринитрат — нитроглицерин (получен в 1847 г. Асканьо Собреро), использующийся в настоящее время в производстве бездымных порохов.
При дегидратации он образует токсичный акролеин:
- HOCH2CH(OH)-CH2OH H2C=CH-CHO + 2 H2O,
и окисляется до глицеринового альдегида СН2ОНСНОНСНО, дигидроксиацетона СН2ОНСОСН2ОН или глицериновой кислоты СН2ОНСНОНСООН.
Эфиры глицерина и высших карбоновых кислот — жиры являются важными метаболитами, важное биологическое значение играют также фосфолипиды — смешанные глицериды фосфорной и карбоновых кислот.
Получение
Глицерин впервые был получен в 1779 году Шееле при омылении жиров в присутствии окислов свинца. Основную массу глицерина получают как побочный продукт при омылении жиров.
Большинство синтетических методов получения глицерина основано на использовании пропилена в качестве исходного продукта. Хлорированием пропилена при 450—500° С получают аллилхлорид, при присоединении к последнему хлорноватистой кислоты образуются хлоргидрины, например, CH2ClCHOHCH2Cl, которые при омылении щёлочью превращаются в глицерин.
На превращениях аллилхлорида в глицерин через дихлоргидрин или аллиловый спирт основаны другие методы. Известен также метод получения глицерина окислением пропилена в акролеин; при пропускании смеси паров акролеина и изопропилового спирта через смешанный ZnO — MgO катализатор образуется аллиловый спирт. Он при 60—70 °C в водном растворе перекиси водорода превращается в глицерин.
Глицерин можно получить также из продуктов гидролиза крахмала, древесной муки, гидрированием образовавшихся моносахаридов или гликолевым брожением сахаров.
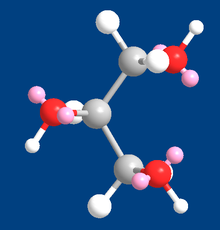 Глицерин (3D модель), показаны атомы и электронные пары при атомах кислорода (розовый цвет)
Глицерин (3D модель), показаны атомы и электронные пары при атомах кислорода (розовый цвет)Триглицериды являются производными глицерина и образуются при присоединении к нему высших жирных кислот. Триглицериды являются важными компонентами в процессе обмена веществ в живых организмах.
Жиры и масла гидрофобны и нерастворимы в воде, так как гидроксильные группы глицерина заменены малополярными остатками жирных кислот.
Применение
Область применения глицерина разнообразна: пищевая промышленность, табачное производство, медицинская промышленность, производство моющих и косметических средств, сельское хозяйство, текстильная, бумажная и кожевенная отрасли промышленности, производство пластмасс, лакокрасочная промышленность, электротехника и радиотехника.
Глицерин используется как пищевая добавка Е422 в производстве кондитерских изделий для улучшения консистенции, для предотвращения проседания шоколада, увеличения объёма хлеба.
Технический глицерин используется для заполнения виброустойчивых манометров типа ДМ8008ВУ, заполнения торцевых уплотнений мешалок и др.
 Реклама глицеринового зубного крема. 1906
Реклама глицеринового зубного крема. 1906См. также
Примечания
Ссылки
На русском и английском языках:
На русском языке:
На английском языке:
Глицерин — Википедия. Что такое Глицерин
Глицери́н (глицерóл, пропантриол-1,2,3) — простейший представитель трёхатомных спиртов с формулой C3H5(OH)3. Представляет собой вязкую прозрачную жидкость.
Свойства
Глицерин — бесцветная, вязкая, очень гигроскопичная жидкость, смешивается с водой в любых пропорциях. Сладкий на вкус, отчего и получил своё название (др.-греч. γλυκός — сладкий). В соединении с пропиленгликолем становится более текучим.
Химические свойства глицерина типичны для многоатомных спиртов.
Взаимодействие глицерина с галогеноводородами или галогенидами фосфора ведёт к образованию моно- и дигалогенгидринов.
Глицерин этерифицируется карбоновыми и минеральными кислородосодержащими кислотами с образованием соответствующих сложных эфиров. Так, с азотной кислотой глицерин образует тринитрат — нитроглицерин (получен в 1847 г. Асканьо Собреро), использующийся в настоящее время в производстве бездымных порохов.
При дегидратации он образует токсичный акролеин:
- HOCH2CH(OH)-CH2OH →{\displaystyle \to } H2C=CH-CHO + 2 H2O,
и окисляется до глицеринового альдегида CH2OHCHOHCHO, дигидроксиацетона CH2OHCOCH2OH или глицериновой кислоты CH2OHCHOHCOOH.
Сложные эфиры глицерина и высших карбоновых кислот — жиры являются важными метаболитами, важное биологическое значение играют также фосфолипиды — смешанные глицериды фосфорной и карбоновых кислот.
Получение
Глицерин впервые был получен в 1779 году Карлом Вильгельмом Шееле при омылении жиров в присутствии окислов свинца[2]. Основную массу глицерина получают как побочный продукт при омылении жиров[3].
Большинство синтетических методов получения глицерина основано на использовании пропилена в качестве исходного продукта. Хлорированием пропилена при 450—500 °С получают аллилхлорид, при присоединении к последнему хлорноватистой кислоты образуются хлоргидрины, например, CH2ClCHOHCH2Cl, которые при омылении щёлочью превращаются в глицерин.
На превращениях аллилхлорида в глицерин через дихлоргидрин или аллиловый спирт основаны другие методы. Известен также метод получения глицерина окислением пропилена в акролеин; при пропускании смеси паров акролеина и изопропилового спирта через смешанный ZnO — MgO катализатор образуется аллиловый спирт. Он при 190—270 °C в водном растворе перекиси водорода превращается в глицерин.
Глицерин можно получить также из продуктов гидролиза крахмала, древесной муки, гидрированием образовавшихся моносахаридов или гликолевым брожением сахаров. Также глицерин получается в качестве побочного продукта при производстве биотоплива.
Производные глицерина и их место в обмене веществ живых организмов
Глицериды
 Глицерин (3D модель), показаны атомы и электронные пары при атомах кислорода (розовый цвет)
Глицерин (3D модель), показаны атомы и электронные пары при атомах кислорода (розовый цвет)Триглицериды являются производными глицерина и образуются при присоединении к нему высших жирных кислот. Триглицериды являются важными компонентами в процессе обмена веществ в живых организмах.
Жиры и масла гидрофобны и нерастворимы в воде, так как гидроксильные группы глицерина заменены малополярными остатками жирных кислот.
Применение
Область применения глицерина разнообразна: пищевая промышленность, табачное производство, электронные сигареты, медицинская промышленность, производство моющих и косметических средств, сельское хозяйство, текстильная, бумажная и кожевенная отрасли промышленности, производство пластмасс, лакокрасочная промышленность, электротехника и радиотехника (в качестве флюса при пайке).
Глицерин относится к группе стабилизаторов, обладающих свойствами сохранять и увеличивать степень вязкости и консистенции пищевых продуктов. Зарегистрирован как пищевая добавка Е422, и используется в качестве эмульгатора, при помощи которого смешиваются различные несмешиваемые смеси.
Поскольку глицерин хорошо поддается желированию и горит без запаха и чада, его используют для изготовления высококачественных прозрачных свечей.
Также глицерин используется при изготовлении динамита[4].
В последние годы глицерин используется, наряду с пропиленгликолем, в качестве основного компонента для приготовления жидкости и картриджей для электронных сигарет.
Используется в криобиологии и крионике как основной компонент популярных проникающих криопротекторов для криоконсервирования анатомических препаратов, биологических тканей и организмов.

Примечания
Ссылки
структурная формула, свойства и области применения :: SYL.ru
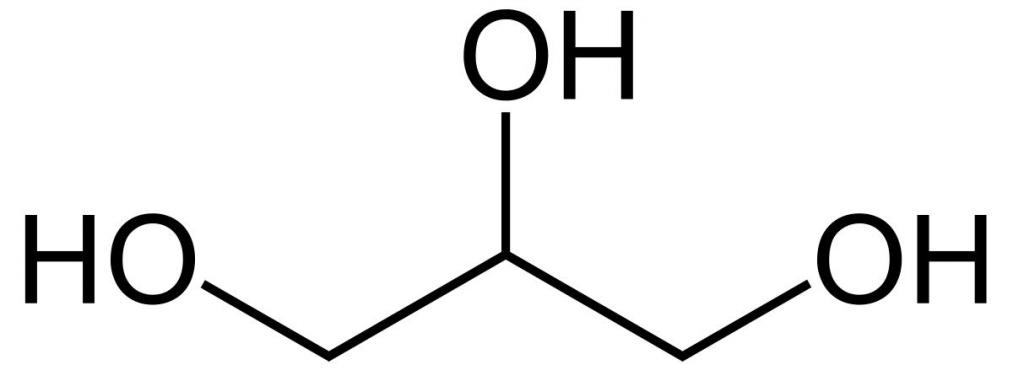
Это простейший трехатомный спирт. Химическая формула глицерина — C3H5(OH)3. Представляет собой прозрачную вязкую жидкость. Не имеет запаха, сладкий на вкус. Он не ядовит, поэтому находит широкое применение в быту, пищевой промышленности, косметике и медицине. Структурная формула глицерина представлена на рисунке. Но как добывают его?
Способы получения глицерина
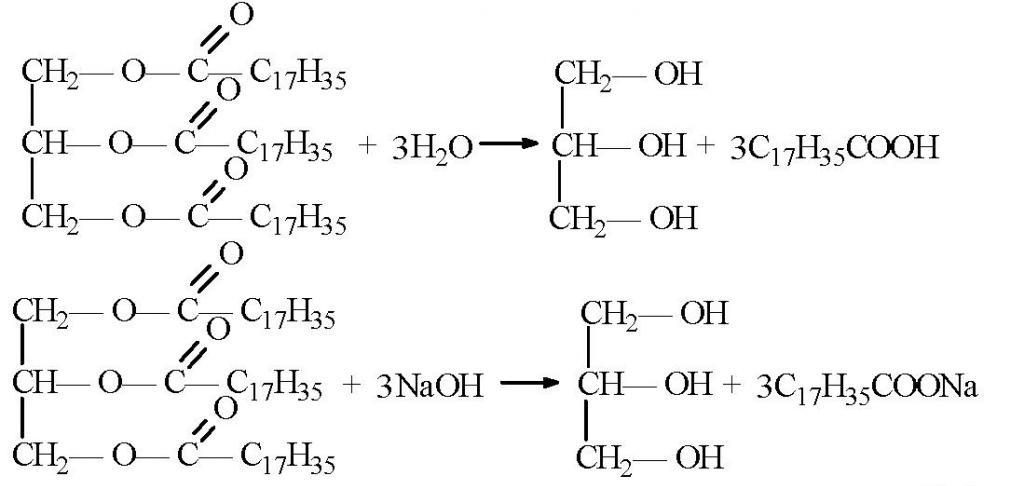
Почти весь глицерин в промышленности получают из жиров. Они с химической точки зрения как раз и представляют собой сложные эфиры глицерина. При омылении этих жиров (получении мыла) глицерин образуется как побочный продукт. Затем он очень просто выделяется из реакционной смеси.
Синтезировать глицерин можно и другими способами. Например, из ацетона. В этом случае его восстанавливают водородом, чтобы получить изопропиловый спирт. На следующей стадии дегидратацией отщепляют молекулу воды, получая пропилен, который затем хлорируют. Полученный дихлорпропан хлорируют еще раз, для получения трихлорпропана. Последняя стадия получения глицерина — гидратация при нагревании. На этой стадии все три молекулы хлора заменяются на гидроксильные группы. Похожим способом сейчас в промышленности получают синтетическое вещество. Только в качестве сырья используют пропилен, который выделяется из побочных газов при перегонке нефти.
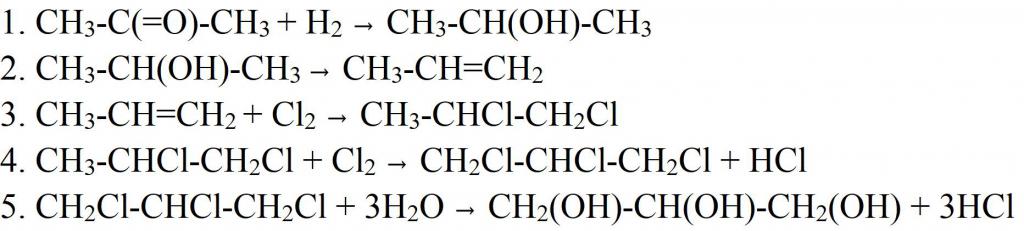
Но из пропилена получать глицерин можно и другим способом. Для этого пропилен окисляют в акролеин. Окисление ведется кислородом воздуха в присутствии катализатора (меди) и повышенной температуре. Далее к нему присоединяют перекись водорода, получая двухатомный спирт-альдегид. В качестве катализатора такой реакции используется оксид осмия (VIII). Альдегидную группу в полученном соединении гидрируют, превращая ее в третью гидроксильную. Так и получается глицерин.
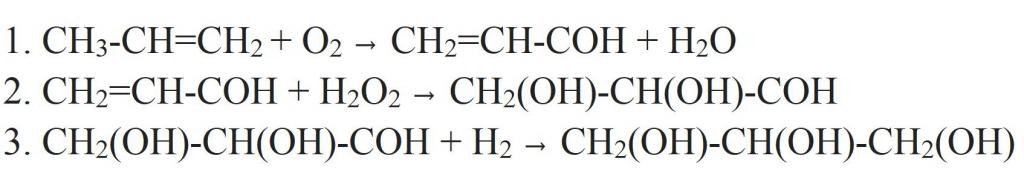
Другой вариант синтеза в свое время предложил Е. Е. Вагнер. Окисляя аллиловый спирт перманганатом калия в щелочной среде, можно в одну стадию получить глицерин.
Физические свойства
Глицерин — бесцветная жидкость без запаха со сладковатым вкусом. Обладает гигроскопичностью, то есть стремится поглощать воду. При температуре 20 °C плавится, а при температуре 290 °C кипит с частичным разложением. Смешивается с водой и спиртами в любых соотношениях. Это обусловлено химической формулой. Гидроксильные группы позволяют глицерину образовывать множество водородных связей с молекулами воды. Это и обеспечивает растворение.
Растворим глицерин также в ацетоне и некоторых других органических веществах. Нерастворим в бензоле и эфирах. Он и сам может является таковым для многих органических и неорганических соединений. Плотность его в жидком состоянии составляет 1,26 г/см3. Также стоит отметить, что глицерин — очень вязкая жидкость. Свойство это в 1474 раза больше, чем у воды.
Химические свойства
Исходя из структурной формулы, глицерин содержит в себе три гидроксильные группы. Поэтому для него будут характерны и химические реакции одноатомных спиртов. Причем кислотные свойства глицерина выражены гораздо сильнее, чем у любого другого одноатомного спирта. Так, он может взаимодействовать с металлами, их оксидами или щелочами. Уравнения химических реакций глицерина представлены ниже.
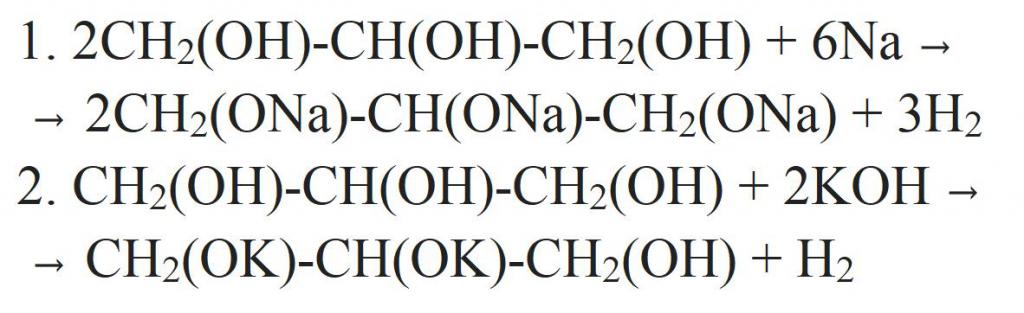
Также он может вступать в реакции дегидратации, образуя множество разных продуктов. Таким образом получают акролеин.
Отдельно стоит сказать про замещение гидроксильной группы на галоген. Это может происходить при взаимодействии глицерина с галогеноводородами. Как видно из структурной формулы глицерина, в результате реакции могут образовываться моно-, ди- и трипроизводные. Более полного замещения можно добиться, если взаимодействие проводить с галогенидами фосфора.
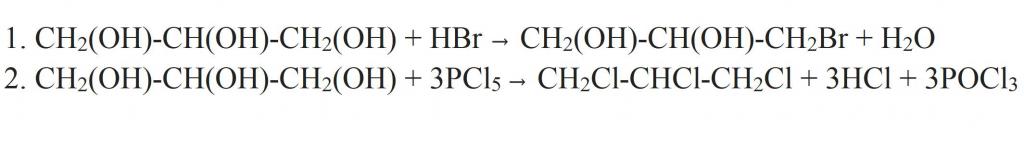
Но глицерин имеет и специфичные свойства, присущие только многоатомным спиртам. Например, он взаимодействует с гидроксидом меди (II), образуя комплексное соединение синего цвета — глицерат меди. Это реакция является качественной для всех многоатомных спиртов.
Характеры для него и реакции этерификации. Это реакция взаимодействия с кислотами, в результате которой получается сложный эфир. Причем этерифицируется глицерин как органическими кислотами, так и минеральными. Например, азотной. Данную реакцию также называют нитрование. В результате нее получается очень полезный, но крайне взрывоопасный продукт — нитроглицерин. Опять же из структурной формулы глицерина видно, что этирифицироваться могут не все гидроксильные группы. Здесь все зависит от условий проведения реакции.
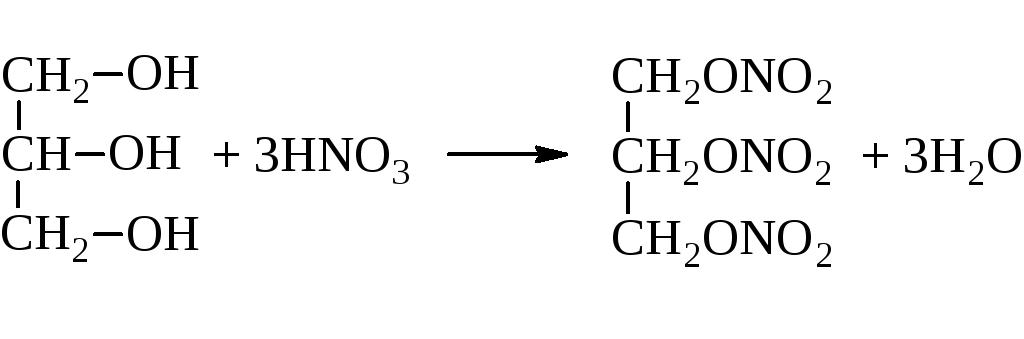
При взаимодействии с водородом при высоком давлении и в присутствии катализторов одна из гидроксильных групп восстанавливается. В результате реакции получается двухатомный спирт — пропиленгликоль.
Глицерин может вступать и в реакции поликонденсации, образуя смесь полиглицеринов. Для этого его очень долго нагревают почти до 300 °C в слабощелочной среде. Химическую формулу глицерина рассмотрели.
Окисление
Очень много у глицерина вариантов окисления. Конечный продукт зависит от природы окислителя, катализаторов и других условий реакции. Так, глицерин можно окислить сильными окислителями, например, дихроматом калия в кислой среде. В результате этой реакции весь глицерин разложится на углекислый газ и воду.
Окисление может происходить и более мягко. Например, при взаимодействии с перекисью водорода получается альдегид или кетон. В качестве катализатора используются соли железа (II).
Окисление можно вести и до получения глицериновой кислоты. В этом случае взаимодействие проводят с концентрированной азотной кислотой. Одна из гидроксильных групп просто окисляется до карбоксильной группы. Из глицерина получают и более экзотические кислоты. При взаимодействии с раствором перманганата калия образуются тартроновая и мезоксалевая кислоты. А при окислении кислородом воздуха с нагреванием в присутствии гидроксида бария получается смесь щавелевой и муравьиной кислоты. Йодной кислотой глицерин можно окислить до муравьиной и формальдегида.
Применение в промышленности
Благодаря своему составу и свойствам, находит глицерин применение в промышленности.
- В текстильной промышленности его используют для придания тканям мягкости и эластичности, а также для синтеза красителей и синтетических волокон.
- Используют его и в производстве некоторых видов бумаги.
- В кожевенной промышленности его растворы применяются для дубления и жировки кожи.
- В сельском хозяйстве с помощью глицерина обрабатывают семена для того, чтобы обеспечить им более стабильное прорастание.
- В лакокрасочной промышленности глицерин применяется для синтеза полировочных составов и лаков.
- При производстве упаковочных материалов, например, целлофана, он используется как пластификатор.
- Полимеры на основе глицерина применяются для производства упаковки. Бумага, пропитанная глицерином, приобретает огнестойкие качества.
Применение в пищевой отрасли
Глицерин — это пищевая добавка Е422. Он используется в качестве стабилизатора для сохранения и увеличения вязкости продуктов. Его применяют в производстве хлебобулочных и кондитерских изделий (особенно шоколада) как загуститель и влагоудерживающий агент. Он помогает придавать объем готовым продуктам. Благодаря этой добавке хлеб может дольше оставаться свежим.
Экстракты на основе глицерина зачастую добавляют в напитки. Они позволяют сделать их вкус менее резким. Также его применяют в производстве алкоголя. Добавляют и в табак, чтобы регулировать влажность, устранять раздражающий привкус.
Применение в медицине
Глицерин входит в состав некоторых препаратов, которые используют при лечении кожных болезней. Он имеет антисептические свойства, препятствует заражению ран. Он также способствует понижению внутричерепного и внутриглазного давления, поэтому его применяют при лечении отека мозга.
Из-за того, что глицерин — хороший растворитель, его активно используют в фармакологической промышленности. С помощью этого вещества можно достигнуть очень высокой концентрации действующего компонента. Также он может придавать нужную консистенцию лекарствам. Его часто добавляют в мази и кремы, ведь тот препятствует выпариванию влаги и высыханию.
Применение в косметологии
Глицерин входит в состав многих косметических средств: мыл, шампуней, кремов, увлажняющих масок. При попадании на кожу в небольших количествах он удерживает влагу в верхних слоях кожи. Однако некоторые утверждают, что частое применение средств с глицериновой основой лишает кожу естественной влаги и лишь усугубляет сухость. Также глицерин часто используют как добавку в мыло. Так увеличивается его моющая способность.
Влияние на организм человека
Глицерин хорошо усваивается организмом, так как легко преобразуется в жиры пищеварительной системой. По этой причине он не считается токсичным. Суточное потребление этого вещества никак не ограничено. Но не стоит забывать, что глицерин гигроскопичен, поэтому в организме он приводит к большому выделению волы, то есть имеется риск наступления обезвоживания. По этой причине применение его в пищевых продуктах строго регламентируется. При попадании на кожу он также оказывает осушающий эффект. До сих пор ведутся споры о необходимости применении вещества в косметических средствах.
Итак, в статье рассмотрели состав и свойства глицерина, его применение.

