Раствор кляйна состав — Здоровье феникса
Раствор Кляйна — анестезиологический раствор, используемый при тумесцентной липосакции. Разработан американским дерматологом Джеффри Кляйном в 1985 году.
Содержание статьи:
Состав раствора Кляйна
В раствор Кляйна входят лидокаин (вызывает местный обезболивающий эффект), адреналин или норэпинефрин (сужает кровеносные сосуды, вследствие чего снижается кровопотеря, уменьшается количество отеков), физиологический раствор (выступает в качестве носителя жира, что позволяет эвакуировать его через канюли) и раствор гидрокарбоната натрия.
Пропорции и количество смеси рассчитываются по формулам для каждого конкретного случая.
Классический рецепт приведён в работе Д.Клайна в двух вариантах:
С использованием местной анестезии
- Литр стерильного физраствора для в/в введения (0.9% NcC1).
- Одна ампула (1 мл) of 1:1,000 эпинефрина.
Раствор Кляйна с анестетиком
Раствор, состоящий из лидокаина (~ 0,1%) и адреналина (~ 1: 1 000 000) в нормальном физиологическом растворе, был приготовлен следующим образом:
- Литр стерильного физраствора для в/в введения (0.9% NcC1).
- Два 50-миллилитровые флакона 1% простого лидокаина (1 gm).
- Одна 1-мл ампула 1:1000 эпинефрина (1 мг эпинефрина).
- Концентрация лидокаина в растворе: 0.091%
- Концентрация эпинефрина в растворе1:1,100,000.[1]
Воздействие раствора Кляйна
Раствор Кляйна вводят под давлением c помощью стандартных шприцев или канюль. Он равномерно распределяется внутри тканей. После ввода раствора необходимо подождать около пятнадцати-двадцати минут. Тогда комбинация компонентов начинает свое действие – сокращаются сосуды и нервные окончания, адипоциты набухают, что облегчает аспирацию. Затем можно начинать процесс ликвидации жировых отложений.
Примечания
- ↑ Jeffrey A. Klein, M.D. The Tumescent Technique for Liposuction Surgery
|
Source: wiki.s-classclinic.com
Читайте также
Раствор кляйна состав пропорции. Раствор кляйна состав
Таблица 5.

Показатели болевых ощущений в группах Применчание. Таблица 6. Распределение пациентов согласно оценке боли по ВАШ. У 1 пациента из группы, А значение боли от 5,1 до 6 см и у 4 из группы Б значение боли от 7,1 до 9 см показатели боли значительно отличались от таковых у остальных испытуемых.
Вопрос №230 — Зачем нужен раствор Кляйна
На наш взгляд, это объясняется крайне низким порогом болевой чувствительности у этих людей. Мы считаем, что болевые ощущения пациентов при проведении тумесцентной анестезии зависят от количества натрия гидрокарбоната, входящего в состав раствора.
При применении небольших доз натрия гидрокарбоната pH рабочего раствора не достигает щелочных значений, поэтому пациенты чувствуют себя не вполне комфортно. Этим могут объясняться результаты некоторых ранее проведенных исследований, в которых разница болевых ощущений между группами пациентов, получавших буферизованный и небуферизованный растворы, оказалась незначимой [14, 17].
В большинстве ранее проведенных исследований средние показатели боли в группах, где анестезию выполняли с использованием буферизованного раствора, находились в интервале от 1,75 до 2,11 см, что несколько выше среднего значения боли у пациентов группы, А в нашем исследовании.
Возможно, это связано с тем, что непосредственно перед инфильтрацией анестетика под кожу мы обезболивали кожу иглой малого диаметра. Согласно рекомендации Д.

Это связано с тем, что буферная емкость зависит от концентрации раствора, но не прямо пропорциональна ей. Следовательно, для растворов, содержащих разное количество лидокаина, необходимо определять точный объем натрия гидрокарбоната, требуемый для достижения слабощелочных значений pH, близких к физиологическим. Но мы рассчитали объем натрия гидрокарбоната только для того количества лидокаина и адреналина, который мы используем в своей практике.
Если же применять другую концентрацию лидокаина или натрия гидрокарбоната, то возникнет необходимость подбора иного количества натрия гидрокарбоната. Хотя среда раствора в нашем исследовании была слабощелочной и не достигала физиологических значений рН 7,35—7,45 , среднее значение боли существенно не отличалось от данных, полученных в недавно проведенном исследовании, в котором для тумесцентной анестезии при выполнении ЭВЛО использовался буферизованный раствор pH 7,4 [27].
Следовательно, нет необходимости доводить pH тумесцентного раствора до физиологических значений, достаточно того, чтобы этот показатель находился в интервале от 7,1 до 7, В таком случае боль при инфильтрации раствора будет уже обусловлена резко щелочной средой раствора.
Так как порог болевой чувствительности у пациентов сильно различается, то в редких случаях мы все же можем ожидать беспокойное поведение пациентов во время анестезии.
Мы считаем, что у такой, хотя и малочисленной, категории необходимо дополнительно применять седативные средства во время операции. Боль, возникающая при проведении тумесцентной анестезии, уменьшается при увеличении pH раствора. Мы не можем повлиять на буферную емкость натрия гидрокарбоната, но можем корректировать количество буфера. Журналы Флебология 1, Снижение выраженности болевого синдро Снижение выраженности болевого синдрома при проведении тумесцентной анестезии: двойное слепое рандомизированное контролируемое исследование Авторы: О.
Букина Стационар одного дня для больных сердечно-сосудистого профиля Областной клинической больницы им.
Ваш дерматолог
Бабенко, Тамбов, Россия А. Баранов кафедра факультетской хирургии Медицинского института Тамбовского государственного университета им.
Державина, Тамбов, Россия. DOI: Просмотрено: Скачано: Список литературы:.
Коррекция фигуры тумесцентной липосакцией
Surgical management of great saphenous vein varicose veins: a metaanalysis. Randomized clinical trial comparing endovenous laser ablation and stripping of the great saphenous vein with clinical and duplex outcome after 5 years. J Vasc Surg. A systematic review and meta-analysis of randomised controlled trials comparing endovenous ablation and surgical intervention in patients with varicose vein.
Тумесцентная липосакция
Сегодня тумесцентная (вакуумная) липосакция широко применяется в пластической хирургии. Благодаря этой процедуре сотни тысяч пациентов смогли убрать лишний жир с разных участков тела и успешно приобрели новые формы лица и тела. В 1985 году Джеффри Кляйн дерматолог из Калифорнии первым провел операцию по липосакции. Являясь разработчиком метода он на практике применил инфильтрацию оперируемой зоны расчетным числом специально созданного им раствора, после чего Кляйн смог удалить жир с живота и бедер. В состав
Пластические хирурги в проведении вакуумной липосакции нацелены на достижение максимального комфорта и безопасности пациентов. Поэтому перед операцией хирург досконально обследует зоны вмешательства и назначает вид анестезии, учитывая индивидуальные особенности организма. В процессе тумесцентной липосакции пациентам зачастую не требуется общая анестезия, достаточно местного обезболивания с одновременным внутривенным введением седативных препаратов. Благодаря применению местной анестезии пациент находится в полном сознании на протяжении всей операции и при этом не испытывает ни боли, ни дискомфорта.
Техника тумесцентной липосакции изначально предполагает применение более тонкой канюли. Это позволяет удалить жир с максимальной безопасностью и при соразмерной инфильтрации операционной зоны существенно снижает риск операционного кровотечения, уменьшает вероятность травмирования нервных волокон, кровеносных сосудов и прилегающей соединительной ткани. Существенно уменьшаются послеоперационные синяки, снижается риск развития сером и гематом.
При использовании тонкой канюли послеоперационные рубцы едва заметны. Хирурги в выборе толщины канюли, безусловно, склоняются в сторону уменьшения ее размеров.
Удаление эмульгированной жировой ткани, необходимо выполнить в полном соответствии с хирургическим планом. Иначе, остатки поврежденных жировых волокон провоцируют возникновение существенных углублений на теле пациента. Беспокойство относительно этого вопроса касается многих, так как на восстановление остатков поврежденных жировых клеток в зоне воздействия может уйти несколько недель. Подобным образом это требование касается точного соблюдения концентрации лидокаина в растворе Кляйна.
После проведения вакуумной липосакции пациенты самостоятельно покидают клинику уже через пару часов, а к повседневному образу жизни могут вернуться спустя 3-4 дня.
То что надо знать о тумесцентной липосакции
Тумесцентная липосакция – усовершенствованная разновидность вакуумной липосакции, в которой ее высокая эффективность сочетается со значительно меньшим уровнем риска и дискомфорта для пациента.
Особенности тумесцентной липосакции
Вакуумная липосакция продолжает оставаться самым действенным методом коррекции фигуры, направленным на избавление от локальных жировых скоплений. Несмотря на появление множества современных вариантов процедуры, значительное количество клиник продолжает практиковать проверенную временем технологию. При реализации практически всех безоперационных протоколов (лазерного, инъекционного, электро- и криолиполиза) адипоциты не удаляются, а всего лишь разрушаются. Последующее выведение образующейся жировой массы возлагается на печень и почки, которые при этом испытывают существенные перегрузки, что может привести к расстройству их функций. Кроме того, такие щадящие варианты липосакции малоэффективны при необходимости извлечения значительного количества ткани. Вместе с тем механическая (вакуумная) экстракция жира удаляет его из организма в большом объеме непосредственно во время операции, не создавая дополнительной работы для внутренних органов. К сожалению, она не лишена существенных недостатков – необходимости общей анестезии, относительно высокого риска развития осложнений и длительного восстановительного периода.
Тумесцентная липосакция
- Физиологический раствор, увеличивающий жировую ткань в объеме за счет набухания, благодаря чему она легко эмульгируется и удаляется экстрактором. При этом существенно снижается травматизация близлежащих структур (сосудов и нервных стволов).
- Лидокаин – средство для местной анестезии, введение которого в клетчатку в большинстве случаев делает ненужным общее обезболивание.
- Адреналин – вещество с сильным сосудосуживающим эффектом. В значительной мере уменьшает операционную кровопотерю и вероятность образования остаточных гематом, а также усиливает действие лидокаина.
Соотношение отдельных препаратов и общий объем раствора рассчитывается по специальной формуле в индивидуальном порядке. Его применяемое количество должно обеспечивать выраженное набухание и разрыхление жировой ткани. Нередко в состав смеси добавляется антибиотик для снижения вероятности инфицирования рабочей зоны. После введения раствора Кляйна под давлением в подкожную клетчатку и выжидания в течение определенного времени (экспозиции) врач приступает к вакуумной экстракции жировой ткани. От классического метода она отличается меньшими разрезами и более тонкой канюлей, что также уменьшает операционную травму.
Противопоказания, предоперационная подготовка, обследование и ход восстановительного периода аналогичны таковым для «обычной» вакуумной липосакции. Главным отличием является существенное сокращение срока реабилитации и значительное снижение операционных рисков.
Достоинства и недостатки метода
Основные преимущества тумесцентной липосакции:
- В большинстве случаев отпадает необходимость в общей анестезии, что избавляет пациента от связанных с ней побочных эффектов (тошноты, рвоты, головной боли).
- Существенно уменьшается операционная кровопотеря.
- Снижается риск травмирования соседних тканей и структур.
- Применяются малые разрезы и тонкие канюли, что улучшает косметический эффект.
- Уменьшается вероятность инфицирования за счет попутного введения антибиотика.
- Послеоперационные гематомы и отеки возникают реже и в меньшем объеме.
- Почти всегда процедура носит амбулаторный характер – пациент вскоре после завершения манипуляции может покинуть клинику.
- Сокращается период различных послеоперационных ограничений, а также срок ношения компрессионного белья.
- Возвращение к активной деятельности происходит уже через несколько дней после вмешательства.
Недостатки:
- Необходимость предварительного расчета, приготовления и введения раствора Кляйна.
- Имеется вероятность передозировки лидокаина с развитием интоксикации.
- Время операции увеличивается по сравнению с классическим методом.
Тумесцентная липосакция – оптимальный вариант оперативного удаления локальных избытков подкожного жира для формирования красивого и пропорционального тела. За счет применения специальной технологии (предварительного введения раствора Кляйна) существенно уменьшается большинство операционных рисков при одновременном сохранении высокой эффективности процедуры.
Уважаемые посетители нашего сайта, если вы делали ту или иную операцию (процедуру) или пользовались каким-либо средством, оставьте пожалуйста ваш отзыв. Он может быть очень полезен нашим читателям!
Раствор для тумесцентной паравазальной анестезии при радиочастотной облитерации вен нижних конечностей
Изобретение относится к области медицины, в частности к хирургии, а именно к растворам для тумесцентной паравазальной анестезии при радиочастотной облитерации вен. Раствор включает физиологический раствор 0,9% в количестве 500,0 мл, 10% лидокаин в количестве 4,0 мл, 5% гидрокарбонат натрия в количестве 25,0 мл. Изобретение обеспечивает высокие анестезирующие свойства и позволяет снизить возможность возникающих осложнений у пациентов за счет исключения адреналина из состава анестезирующего раствора. 2 пр.
Изобретение относится к области медицины, в частности, к хирургии, а именно к способам анестезии, и может быть использовано при проведении флебологических операций на нижних конечностях.
Варикозное поражение вен регистрируется среди различных контингентов населения. В развитых странах мира частота варикозной болезни составляет 25-33% среди женщин и 10-20% среди мужчин. В России только официально зарегистрировано более 38 млн. человек, страдающих различными формами варикозной болезни, из которых у 15% имеются трофические расстройства. Количество людей, страдающих заболеваниями вен, ежегодно увеличивается на 2,5% [http: travma-net.ru>Articles, aspx…].
В настоящее время большая часть современных эндовенозных операций выполняется под местной тумесцентной анестезией. Паравазальная блокада местными анестетиками обеспечивает надежное обезболивание нижних конечностей. При правильном проведении тумесцентная паравазальная анестезия обеспечивает адекватное обезболивание, мышечную релаксацию и надежно защищает окружающие ткани от воздействия термического фактора с минимальным влиянием на жизненно важные функции пациента.
Радиочастотная абляция вен (радиочастотная облитерация вен, РЧА, VNUS) — является одной из современных методик лечения варикозного расширения вен нижних конечностей, включающей воздействие радиочастотного излучения (токов высокой частоты) на внутреннюю поверхность вены, вызывая коагуляцию. В результате этого происходит закрытие просвета кровеносного сосуда (облитерация), а в дальнейшем его полное рассасывание (абляция).
В процессе радиочастотной абляции вен широко используется периферическая регионарная анестезия [Айзенберг В.Л., Цыпина Л.Е., Ледяной Г.Ф., Овчинникова В.И. Регионарная анестезия сплетений у детей с использованием нейростимулятора Stimuplex HNS 11. http://anesth.medi.ru/omskyomsk7003.htm].
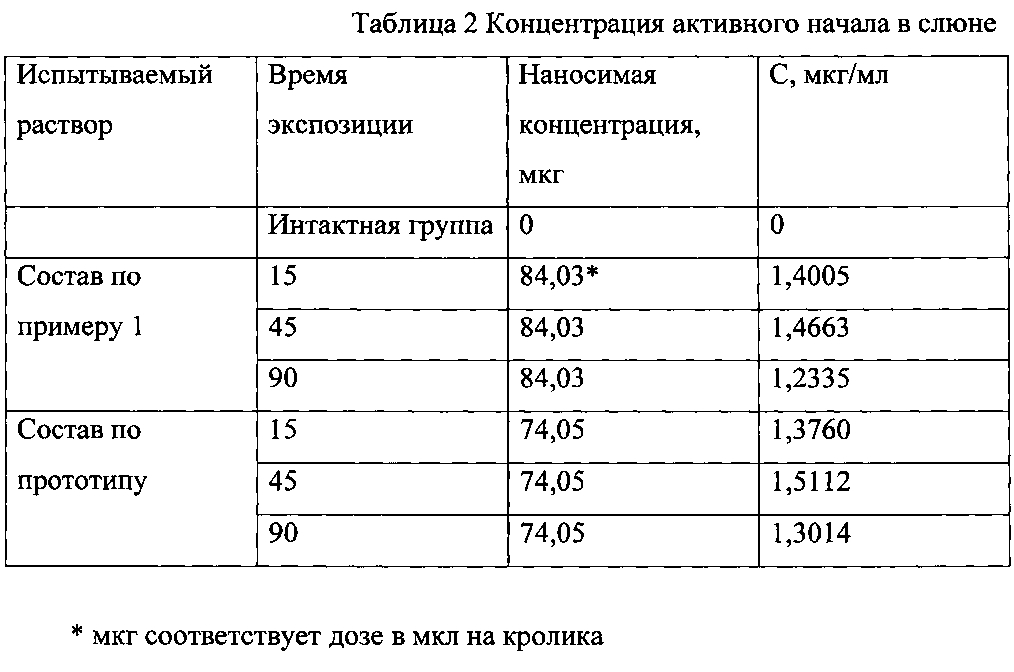
В качестве прототипа нами выбран широко применяемый для периферической регионарной анестезии раствор, предложенный Кляйном (Klein). Раствор готовится на физиологическом растворе (1000 мл) с добавлением 1% лидокаина с адреналином (100 мл) и 8,4% раствора гидрокарбоната натрия (10 мл) [криз.рф/archives/748].
Предложенный раствор для тумесцентной анестезии при радиочастотной облитерации вен нижних конечностей имеет следующие недостатки: адреналин, входящий в состав стандартного раствора Кляйна, пролонгирует действие лидокаина, который часто вызывает побочные нарушения в организме, а именно, нарушение сердцебиения, головную боль, головокружение, аллергические проявления и др.
Задачей настоящего изобретения является создать раствор для тумесцентной паравазальной анестезии при радиочастотной облитерации вен нижних конечностей, позволяющий наряду с высокими анестезирующими свойствами снизить побочные эффекты, возникающие в организме пациента.
Технический результат — простой, не требующий материальных затрат и основан на исключение адреналина из состава анестезирующего раствора.
Раствор для тумесцентной паравазальной анестезии при радиочастотной облитерации вен нижних конечностей согласно технического решения содержит следующие компоненты: физиологический раствор 0,9% в количестве 500,0 мл, 10% лидокаин в количестве 4,0 мл и 5% гидрокарбоната натрия в количестве 25,0 мл.
Предложенный раствор используют следующим образом.
После обработки операционного поля в области истока большой подкожной вены слева выполняют линейный разрез до 0,5 см, в проксимальный конец вены вводят радиочастотный катетер под контролем ультразвукового ангиосканирования (УЗИ), отступив на 2 см от сафено-феморального соустья. Затем выполняют тумесцентную паравазальную анестезию предложенным раствором на всем протяжении большой подкожной вены. После анестезии осуществляют эндовенозную посегментную радиочастотную облитерацию вены. Накладывают шов на рану, асептическую повязку и компрессионный трикотаж II класса компрессии.
Сущность тумесцентной паравазальной анестезии заключается в том, что обезболивание проводят паравазально, т.е. анестезирующий раствор вводят непосредственно около сосуда, в котором расположен радиочастотный катетер. Ход операции контролируют результатами проведения УЗИ.
Примеры практического использования предлагаемого способа.
Пример 1.
Больная А., 47 лет. Диагноз: Хроническое заболевание вен левой нижней конечности C2,3,4S,Ep,As,Pr; 23.01.2017; LI. ХВН II степени. Операция 23.01.2017 г. Радиочастотная облитерация ствола БПВ слева на всем протяжении.
С лечебной целью использован раствор для тумесцентной паравазальной анестезии при радиочастотной облитерации вен нижних конечностей, содержащий следующие компоненты: физиологический раствор 0,9% в количестве 500,0 мл, 10% лидокаин в количестве 4,0 мл и 5% гидрокарбоната натрия в количестве 25,0 мл.
После обработки операционного поля в области истока большой подкожной вены слева выполнен линейный разрез до 0,5 см, в проксимальный конец вены введен радиочастотный катетер под контролем ультразвукового ангиосканирования, отступя 2 см от сафено-феморального соустья. Затем выполнена тумесцентная паравазальная анестезия предложенным раствором на всем протяжении большой подкожной вены. Затем эндовенозная посегментная радиочастотная облитерация вены. Наложен шов на рану. Асептическая повязка. Компрессионный трикотаж II класса компрессии.
Послеоперационный период протекал без особенностей. Больная находилась в хирургическом отделении 2 часа. Выписана в удовлетворительном состоянии в день операции. В течение 6 месяцев у больной постоперационных осложнений не наблюдалось.
Пример 2.
Больной Н., 28 лет. Диагноз: Хроническое заболевание вен нижних конечностей C2,3,4,6S,Ep,As,Pr; l8.06.2016; LI. ХВН II степени. Операция 18.06.2017 г. Радиочастотная облитерация ствола БПВ справа и слева на всем протяжении.
С лечебной целью использован раствор для тумесцентной паравазальной анестезии при радиочастотной облитерации вен нижних конечностей, содержащий следующие компоненты: физиологический раствор 0,9% в количестве 500,0 мл, 10% лидокаин в количестве 4,0 мл и 5% гидрокарбоната натрия в количестве 25,0 мл.
После обработки операционного поля в области истока большой подкожной вены слева выполнен линейный разрез до 0,5 см, в проксимальный конец вены введен радиочастотный катетер под контролем ультразвукового ангиосканирования, отступя 2 см от сафено-феморального соустья. Затем выполнена тумесцентная паравазальная анестезия предложенным раствором на всем протяжении большой подкожной вены. Выполнена эндовенозная посегментная радиочастотная облитерация вены. Наложен шов на рану. Аналогичным образом выполнена операция на стволе правой БПВ. Наложена асептическая повязка и компрессионный трикотаж II класса компрессии.
На весь период операции использован 1 литр анестезирующего раствора.
Послеоперационный период протекал без особенностей. Больной находился в хирургическом отделении сутки. Выписан в удовлетворительном состоянии на следующий день после операции. В течение 6 месяцев у больного постоперационных осложнений не наблюдалось.
Предложенный состав раствора для проведения обезболивания внедрен на базе: Частное учреждение здравоохранения «Клиническая больница» («РЖД-Медицина» г. Тюмень»). При оперативном лечении варикозной болезни нижних конечностей использован анестезирующий раствор, содержащий следующие компоненты: физиологический раствор 0,9% в количестве 500,0 мл, 10% лидокаин в количестве 4,0 мл, 5% гидрокарбонат натрия в количестве 25,0 мл. Проведено более 50 операций. Послеоперационные осложнения не наблюдались.
Раствор для тумесцентной паравазальной анестезии при радиочастотной облитерации вен нижних конечностей включает следующие компоненты: физиологический раствор 0,9% в количестве 500,0 мл, 10% лидокаин в количестве 4,0 мл, 5% гидрокарбонат натрия в количестве 25,0 мл.
Виды липосакции | Здоровье и Красота
Виды липосакции…
Давайте разберемся, какие же виды липосакции существуют.
Классическая липосакция
У классической липосакции есть две разновидности: влажная липосакция и сухая липосакция.
Сухая липосакция
При сухой липосакции не осуществляется обкалывание поля операции местным анестетиком перед удалением подкожно-жировой клетчатки. Он относится к достаточно травматичным методикам и, как правило, сопровождается обильной кровопотерей.
Влажная липосакция
При влажной липосакции вводится различное количество жидкости, которая представляет из себя смеси солевых растворов, местных анестетиков (обычно используется лидокаин) и адреналина (препарата, который суживает сосуды), и уже после разжижения подкожно-жировой клетчатки происходит ее удаление. Благодаря этому уменьшается травматизм мягких тканей, уменьшается кровопотеря и обеспечивается эффект обезболивания в интра- и постоперационном периоде.
С появлением новейших технологий и усовершенствования методов классической липосакции, в медицинскую практику были внедрены несколько вариантов липосакции.
Каждый из этих вариантов имеет свои недостатки и достоинства, и, как следствие, имеют свои противопоказания и свои показания. В связи с чем оперирующий хирург осуществляет выбор методики отталкиваясь от индивидуальных особенностей пациента.
Тумесцентная липосакция
В недалеком 1985-м году врач Джеффри Кляйн, а также врач Патрик Лиллисом, описали методику тумесцентной липосакции (от английского слова «tumescent», что означает «распухающий»). При тумесцентной липосакции в зону поля операции заблаговременно вводят обильные объемы раствора Кляйна (который иногда раза в три превышает объем удаляемой подкожножировой клетчатки).
В состав раствора Кляйна входят: раствор физиологический, лидокаин, адреналин, в пропорциях, рассчитывающихся по специальным формулам. Данный раствор вводится под сильным давлением, результатом чего является набухание адипоцитов (клеток подкожно-жировой клетчатки), благодаря чему последующий процесс их удаления упрощается.
Перед удалением выжидают 30-ть — 60-т минут. Из-за того, что в растворе Кляйна содержится достаточно большое количество местного анестетика, необходимость в дополнительной анестезии отсутствует. Поэтому тумесцентная липосакция проводится, как правило, людям, которым необходима местная анестезия, но на эту методику тратится больше времени, чем на классическую липосакцию.
Ультразвуковая липосакция
Ультразвуковая липосакция — это липосакция, при которой используется специальный ультразвуковой зонд. От воздействия волн ультразвуковой частоты происходит разрыв клеток подкожно-жировой клетчатки и они превращаются в жировую эмульсию. После чего, посредством тонких канюль и отсоса, происходит удаление жира.
Благодаря ультразвуковой липосакции упростилось выполнение, а также увеличилась эффективность операции липосакции в «фиброзных» зонах тела человека (к примеру, липосакция на увеличенной в размерах мужской груди). Но, при этой процедуре выделяется большое количество тепловой энергии (вспомните микроволновую печь), что может привести к ожогам кожных покровов.
Чтобы этого не происходило, операционное поле обкалывается раствором Кляйна («тумесцентным раствором»). Но это тоже приводит к некоторым недостаткам: из-за перерастяжения тканей тяжело контролировать количество удаляемой подкожно-жировой клетчатки.
По времени эта методика длится дольше, чем классическая липосакция, и может приводить к таким нежелательным осложнениям, как ожоги кожных покровов и серомы.
Раствор Рингера — Википедия
Раство́р Ри́нгера — многокомпонентный физиологический раствор. Раствор в дистиллированной воде нескольких неорганических солей с точно выдержанными концентрациями, таких как хлорид натрия, хлорид калия, хлорид кальция, а также бикарбонат натрия для стабилизации кислотности раствора pH как буферный компонент.
Применяется в медицине, в физиологии для изучения деятельности тканей вне органов, для перфузии изолированных органов.
Иногда в составы раствора Рингера, используемые в физиологии, могут вводиться питательные вещества для живых тканей, например, АТФ, глюкозу, а также для подавления развития вредной микрофлоры антибиотики и противогрибковые средства.
Стандартный раствор Рингера состоит из 6,5 г NaCl, 0,42 г KCl и 0,25 г CaCl2 растворённых в 1 литре бидистиллированной (в стеклянном перегонном аппарате) воды.
Раствор был назван в честь Сиднея Рингера, который в 1882—1885 годах установил, что в растворе для перфузии сердца лягушки должны содержаться соли натрия, калия и кальция в найденной им пропорции, чтобы изолированное сердце лягушки продолжало биться в течение длительного времени[1].
В составе медицинского раствора Рингера содержится 8,60 г NaCl, 0,30 г KCl и 0,33 г CaCl2 на литр и вспомогательные вещества — едкий натр, соляная кислота. Раствор содержит: натрия (Na+) 147,00 ммоль, калия (K+) 4,00 ммоль, кальция (Ca2+) 2,25 ммоль, хлоридa (Cl—) 155,60 ммоль. Теоретическая осмолярность: 309 мосмоль.[2]
Раствор Рингера возмещает потери экстрацеллюлярной жидкости и основных электролитов (натрия, калия, кальция) и хлоридов.
Вводят внутривенно капельно в дозе от 500 до 1000 мл /сутки, средняя скорость введения — 3,0 мл/кг массы тела в час или 70 капель/мин или 250 мл/час. Общая суточная доза составляет до 2-6 % массы тела.
Показания к применению[править | править код]
В качестве плазмозамещающего средства при отсутствии необходимости в возмещении эритроцитов, в том числе при шоке, коллапсе, ожогах, обморожениях, длительной рвоте, диарее. Препарат используют при дегидратации различного генеза, гипонатриемии, гиповолемическом шоке (как вспомогательная терапия), при метаболическом ацидозе с потерей жидкости.
Противопоказания[править | править код]
Гиперчувствительность к компонентам препарата, декомпенсированная сердечная недостаточность, отек легких, отек мозга, олигоурия, анурия, ацидоз, гиперволемия, гиперхлоремия, гиперкальциемия, гипернатриемия, сопутствующая терапия ГКС.
С осторожностью — при сердечной недостаточности, артериальной гипертензии, нарушение функции печени или почек.
Побочные действия[править | править код]
При введении большого объема раствора возможно развитие ацидоза.
При неадекватно высокой дозе возможно нарушение водно-электролитного баланса, в том числе гиперволемия, гипернатриемия, гиперкалиемия, гиперкальциемия, гиперхлоремия.
Растворы Рингера в физиологии животных[править | править код]
В физиологии животных используются растворы Рингера несколько иного состава:
| Ингредиент | для млекопитающих | для лягушек | для насекомых |
|---|---|---|---|
| NaCl | 0,9 % | 0,650 % | 0,650 % |
| KCl | 0,042 % | 0,014 % | 0,025 % |
| CaCl2 | 0,024 % | 0,012 % | 0,025 % |
| NaHCO3 | 0,015 % | 0,020 % | 0,025 % |
Является разновидностью раствора Рингера. Состав: 25 mM NaCl, 2,5 mM KCl, 1,25 mM NaH2PO4, 2 mM CaCl2, 1 mM MgCl2, 25 mM NaHCO3, 25 mM глюкоза. Аэрация карбогеном (95 % O2 и 5 % CO2) в течение 30 минут для достижения физиологического pH 7,4[3].
Является разновидностью раствора Рингера. Применяется в медицине, в физиологии для изучения деятельности тканей вне организма, для перфузии изолированных органов. Представляет собой бесцветный прозрачный водный раствор следующего состава[4]:
Раствор Рингера—Локка изотоничен плазме крови животных, регулирует водно-солевое и кислотно-щелочное равновесие в организме животных. После введения препарата быстро всасывается из места инъекции и распределяется в органах и тканях животного.
По степени воздействия на организм Раствор Рингера—Локка согласно ГОСТ 12.1.007-76 относится к веществам малоопасным (4 класс опасности). Препарат не оказывает раздражающего действия на ткани.
Срок годности препарата — 2 года со дня изготовления. Запрещается использовать лекарственное средство после окончания срока его годности.
Показания к применению: шок, отравления, ожоги, холера, токсическая диспепсия, неукротимая рвота, острые кровопотери (вместе с гемотрансфузией).
Одна из разновидностей раствора Рингера. Применяется в медицине, в физиологии для изучения деятельности тканей вне органов, для перфузии изолированных органов.
| Ингредиент | % |
|---|---|
| NaCl | 0,800 |
| KCl | 0,020 |
| CaCl2 | 0,020 |
| NaHCO3 | 0,010 |
| MgCl2 | 0,010 |
| NaH2PO4 | 0,005 |
| Глюкоза | 0,100 |
Раствор Tyrode для теплокровных (37 °C)[5]:
| Ингредиент | n, ммоль | мол. вес | c, моль/л | V, мл | m, г |
|---|---|---|---|---|---|
| NaCl | 135 | 58,44247 | 4 | 33,75 | 7,88973345 |
| KCl | 4 | 74,551 | 1 | 4 | 0,298204 |
| Nah3PO4*2h3O | 0,33 | 192 | 1 | 0,33 | 0,06336 |
| MgCl2*6h3O | 1 | 203,3007 | 1 | 1 | 0,2033007 |
| Глюкоза | 11 | 180 | 10 | 1,1 | 1,98 |
| CaCl2*2h3O | 2,5 | 110,9834 | 1 | 2,5 | 0,2774585 |
| HEPES (4-(2-hydroxyethyl)-1-piperazineethanesulfonic acid) | 10 | 260 | нет | нет | 2,6 |
0,15—0,3 % коллагеназа (Sigma тип IV) до pH=7,3.
Концентрация c, моль/л указана для приготовления матричных растворов (тогда, когда это возможно) для последующего их дозирования по объему (V, мл), что ускоряет процесс приготовления растворов.[источник не указан 352 дня]

